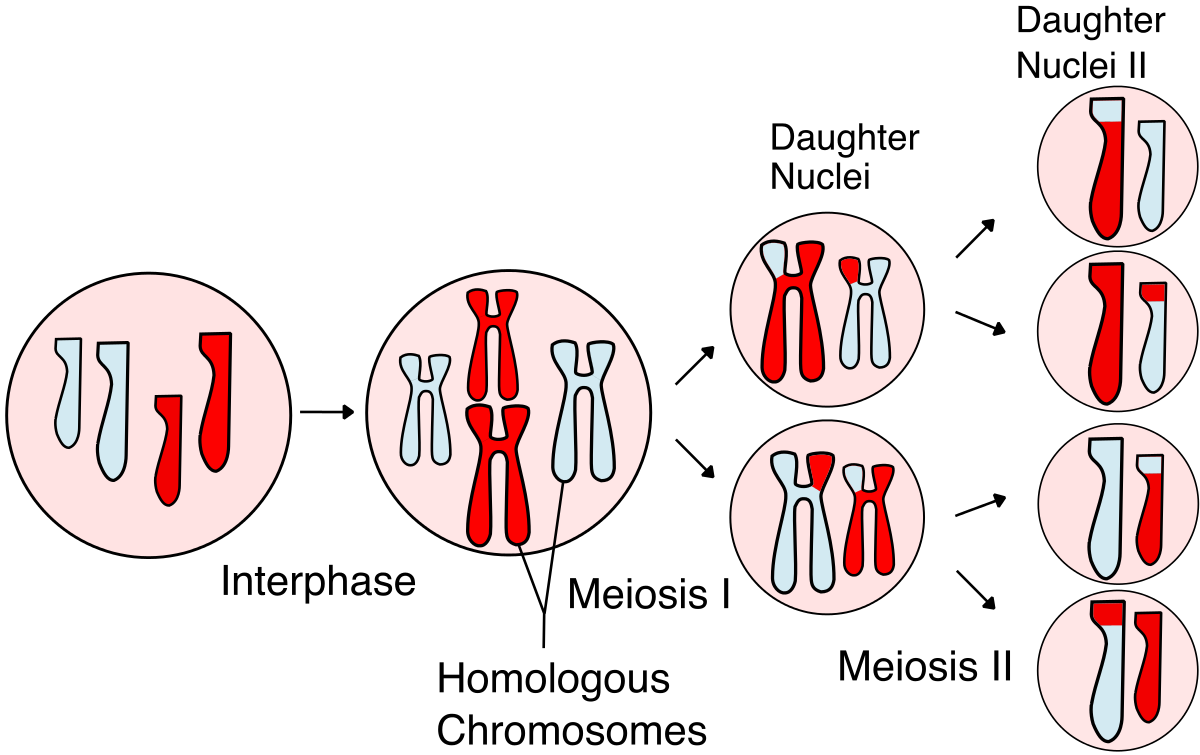
মৌলসমূহের শ্রেণিবিভাগ ও পর্যায়বৃত্ত ধর্ম
দেশের সরকারি-বেসরকারি কলেজ সমূহ থেকে ২০২১ সালের এইচএসসি পরীক্ষায় অংশগ্রহণকারী শিক্ষার্থী বন্ধুরা তোমাদের জন্য আজ ২০২১ সালের এসএসসি পরীক্ষার্থীদের জন্য ৪র্থ সপ্তাহের রসায়ন প্রথম পত্র অ্যাসাইনমেন্ট মৌলসমূহের শ্রেণিবিভাগ ও পর্যায়বৃত্ত ধর্ম সম্পর্কে বিস্তারিত আলোচনা নিয়ে এলাম। এটি অনুসরণ করে তোমরা চতুর্থ সপ্তাহে এইচএসসি ২০২১ সালের রসায়ন প্রথম পত্র এসাইনমেন্ট কি খুব ভালোভাবে সমাধান করতে পারবে এবং মূল্যায়নের সর্বোচ্চ নম্বর পাবে।
আজকে তোমাদের জন্য ২০২১ সালের এসএসসি পরীক্ষার্থীদের চতুর্থ সপ্তাহে রসায়ন পাঠ্যবই থেকে নির্ধারিত অ্যাসাইনমেন্টের প্রশ্নসমূহের ধারাবাহিকতা বজায় রেখে মূল্যায়ন রুবিক্স অনুসরণ করে একটি সেরা উত্তর সমাধান দেয়ার চেষ্টা করা হবে।
এইচএসসি ২০২১ চতুর্থ সপ্তাহ রসায়ন ১ম পত্র অ্যাসাইনমেন্ট সমাধান
এই আলোচনা শেষে তোমরা যে সকল প্রশ্নের উত্তর লিখতে পারবে তা নিচে দেয়া হল-
ক) ইলেকট্রন বিন্যাসের ভিত্তিতে পর্যায় সারণির মৌলসমূহের শ্রেণিবিভাগ বর্ণনা;
খ) পর্যায় সারণির একই পর্যায়ের মৌলসমূহের আয়নিকরণ শক্তির পরিবর্তন ব্যাখ্যা;
গ) পর্যায় সারণির একই শ্রেণিতে মৌলসমূহের ইলেকট্রন আসক্তির পরিবর্তন ব্যাখ্যা;
ঘ) মৌলের তড়িৎ ঋণাত্বকতার উপর বিভিন্ন নিয়ামকের প্রভাব ব্যাখ্যা;

মৌলসমূহের শ্রেণিবিভাগ ও পর্যায়বৃত্ত ধর্ম
বন্ধুরা তোমাদের জন্য 21 সালের এইচএসসি পরীক্ষার্থীদের চতুর্থ সপ্তাহে বিজ্ঞান বিভাগের রসায়ন প্রথম পত্র অ্যাসাইনমেন্ট মৌল সমূহের শ্রেণীবিভাগ ও পর্যায়বৃত্ত ধর্ম সম্পর্কে বিস্তারিত আলোচনার মাধ্যমে প্রশ্নসমূহের উত্তর দেয়া হয়েছে।
ক) ইলেকট্রন বিন্যাসের ভিত্তিতে পর্যায় সারণির মৌলসমূহের শ্রেণিবিভাগ;
ক এর উত্তর
আধুনিক পর্যায় সারণির বিভিন্ন মৌলকে তাদের বহিঃস্থ বা যোজ্যতা স্তরের ইলেকট্রন বিন্যাস অনুযায়ী চারটি ব্লকে ভাগ করে সাজানো হয়েছে। যেখানে মূল ভিত্তি হিসেবে ইলেকট্রন বিন্যাস কাজ করে। পর্যায় সারণির মৌলসমূহের চারটি ব্লক যথাক্রমে ১) s ব্লক ২) p ব্লক ৩) d ব্লক ৪) f ব্লক। নিচে পর্যায় সারণির মৌলসমূহের ইলেকট্রন বিন্যাস এর ভিত্তিতে আলোচনা করা হলো-
১) s ব্লক মৌল: যে সব মৌলের ইলেকট্রন বিন্যাস এর সর্বশেষ ইলেকট্রন টি s অরবিটালের ভিতরে প্রবেশ করে তাদেরকে s ব্লক মৌল বলা হয়। পর্যায় সারণির গ্রুপ IA এবং IIA গ্রুপ এর মৌল সমূহ এবং 0 গ্রুপের He মৌলটি s ব্লকের অন্তর্ভুক্ত। s ব্লক মৌলের সংখ্যা 14 টি। এদের পরমাণুর বহি স্তরের ns1, ns2
যেমন: Li(3)=1s2 2s1
২) p ব্লক মৌল: যে সব মৌলের ইলেকট্রন বিন্যাসের সর্বশেষ ইলেকট্রন p অরবিটালে প্রবেশ করে তাদেরকে p ব্লক মৌল বলা হয়। পর্যায় সারণির গ্রুপ IIIA থেকে গ্রুপ VIIA এর মৌলসমূহ এবং 0 গ্রুপের হিলিয়াম ছাড়া অবশিষ্ট মৌলসমূহ p ব্লকের অন্তর্ভুক্ত। এদের পরমাণুর বহিস্তরের গঠন ns2, ns1-6
যেমন: O(8)=1s2 2s2 2p6; Ne (10)=1s2 2s2 2p6;
৩) d ব্লক মৌল: যে সব মৌলের ইলেকট্রন বিন্যাস এর সর্বশেষ ইলেকট্রনটি d অরবিটাল প্রবেশ করে তাদেরকে d ব্লক মৌল বলা হয়। পর্যায় সারণির B উপস্তরের মৌলসমূহ এবং গ্রুপ VIII এর মৌল সমূহ d ব্লকের অন্তর্ভুক্ত। এদের সাধারণ ইলেকট্রন বিন্যাস (n-1) d1-10 ns1-2 এই সবগুলোই ধাতু।
অবস্থান্তর মৌল: যেসব d-ব্লক মৌল এর স্থিতিশীল আয়নে অপূর্ন d অরবিটাল d1-9 উপস্থিত থাকে, তাদেরকে অবস্থান্তর মৌল বলা হয়। উদাহরণস্বরূপ Fe একটি অবস্থান্তর মৌল।
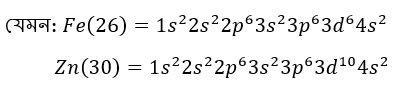
অতএব, Zn অবস্থান্তর মৌল নয় তবে Fe অবস্থান্তর মৌল।
৪) f ব্লক মৌল: যেসব মৌলের ইলেকট্রন বিন্যাস এর সর্বশেষ ইলেকট্রনটি অভ্যন্তরীণ স্তরের f অরবিটালে প্রবেশ করে ,তাদেরকে f ব্লক মৌল বলে।
ষষ্ঠ পর্যায় ও গ্রুপ IIIA তে অবস্থিত ল্যান্থানাম (La) থেকে পরবর্তী লুটিয়াম(Lu) পর্যন্ত 15 টি মৌলকে ল্যান্থানাইড শারিতে এবং 7 পর্যায় ও গ্রুপ IIIB তে অবস্থিত অ্যাক্টিনিয়াম(Ac) থেকে পরবর্তী লরেন্সিয়াম(Lr) পর্যন্ত 15 টি অ্যাক্টিনাইড শারিতে স্থান দেওয়া হয়েছে। f ব্লক মৌল সমূহের বহিস্ত স্তরে ইলেকট্রনীয় গঠন: (n-2)f1-14 (n-1) d0,1 ns2 এগুলোকে পর্যায় সারণির নিচে আলাদাভাবে স্থান দেওয়া হয়েছে।
খ) পর্যায় সারণির একই পর্যায়ের মৌলসমূহের আয়নিকরণ শক্তির পরিবর্তন ব্যাখ্যা
খ এর উত্তর
গ্যাসীয় অবস্থায় এক মোল বিচ্ছিন্ন পরমাণু থেকে ইলেকট্রন অপসারণ এর মাধ্যমে গ্যাসীয় এক মোল একক ধনাত্মক আয়নে পরিণত করতে যেই শক্তির প্রয়োজন হয়, তাকে ওই মোলের আয়নীকরণ শক্তি বলে।
আয়নিকরণ শক্তি পর্যায়ভিত্তিক ধর্ম অনুসারে পরিবর্তিত হয়। একই পযায়এর বাম থেকে ডানে পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে ইলেকট্রন শক্তিস্তর এর সংখ্যা বাড়ে না, তবে উপশক্তিস্তর সংখ্যা বাড়ে , এতে নিউক্লিয়াস থেকে বহিঃস্থ ইলেকট্রনের দূরত্ব কমে যায়পরমাণুর আকার হ্রাস পায়, নিউক্লিয়াসে ধনাত্মক চার্জ বৃদ্ধির ফলে সর্ববহিঃস্থ ইলেকট্রন অধিকতর আকৃষ্ট হয়।
ফলে ইলেকট্রন অপসারণের জন্য অধিক শক্তির প্রয়োজন, তাই এতে করে একই পর্যায়ের বাম থেকে ডানে গেলে মৌলের আয়নিকরণ শক্তি বাড়ে। তবে এতে কিছু ব্যতিক্রম লক্ষ্য করা যায়। তারমধ্যে Beও Bএবং N ও Oএর ক্ষেত্রে আয়নীকরণ শক্তিমানের ব্যতিক্রম পরিলক্ষিত হয়। নিচে তা ইলেকট্রন বিন্যাসের মাধ্যমে ব্যাখ্যা করা হলো।
আয়নীকরণ সংজ্ঞা মতে বেরিলিয়ামের আয়নিকরণ শক্তি বোরন অপেক্ষা কম হওয়ার কথা কিন্তু ইলেকট্রন বিন্যাস লক্ষ করলে দেখা যায় যে বেরিলিয়াম এর ইলেকট্রন বিন্যাস সুস্থিত যেখানে বোরনের ইলেকট্রন বিন্যাস এর শেষ শক্তিস্তরে একটি ইলেকট্রন বিজোড় অস্থিতিশীল অবস্থায় রয়েছে ।
যার ফলে বোরনের শেষ ইলেকট্রন টি কে. অতি সহজে অপসারণ সম্ভব। যেখানে বেরিলিয়ামের সর্বস্তরের ইলেকট্রন অপসারণ করতে আরো বেশি শক্তি প্রয়োজন। ইলেকট্রন বিন্যাস খেয়াল করলে দেখা যায়-
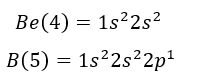
B এর 2p স্তরের বিজোড় ইলেকট্রন এর কারণে কম শক্তির ফলে বোরণের শক্তিস্তর থেকে শেষ ইলেকট্রন অপসারণ সম্ভব। আর তাই বেরিলিয়াম অপেক্ষা বোরণের আয়নীকরণ শক্তি কম।
আয়নীকরণ সংজ্ঞা মধ্যে অক্সিজেনের আয়নীকরণ মান নাইট্রোজেন অপেক্ষা বেশি হওয়ার কথা। তবে ইলেকট্রন বিন্যাস বিজোড় ইলেকট্রন স্থায়িত্ব তার কারন এ নাইট্রোজেনের আয়নিকরণ শক্তি অক্সিজেন থেকে বেশি।
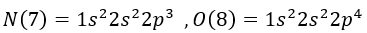
নাইট্রোজেন এবং অক্সিজেনের ইলেকট্রন বিন্যাস লক্ষ্য করলে দেখা যায় নাইট্রোজেনের ইলেকট্রন সমূহ অর্ধপূর্ণ অবস্থায় রয়েছে। যেখানে অক্সিজেনের শক্তিস্তরের ইলেকট্রনসমূহ অর্ধপূর্ণ বা পূর্ণ অবস্থায় নেই। এবং তাই নাইট্রোজেন থেকে সর্বশেষ যে কোন ইলেকট্রন অপসারণ ,অক্সিজেন এর সর্বশেষ ইলেকট্রন অপসারণের থেকে বেশি শক্তি প্রয়োজন।
আমরা জানি, কোন মৌলের ইলেকট্রন বিন্যাসে তা অর্ধপূর্ণ বা পূর্ণ অবস্থায় অধিকতর স্থায়ী অবস্থা বিদ্যমান। অতএব উভয় মৌল এর ইলেকট্রন বিন্যাসের আয়নিকরণ শক্তির মানের ব্যতিক্রম এর কারণ মৌলসমূহের পূর্ণ বা অর্ধপূর্ণ ইলেকট্রন বিন্যাসের স্থায়িত্ব। অতএব তাদের ব্যতিক্রমী আয়নিকরণ শক্তির ক্রম হবে N>O এবং Be>B
গ) পর্যায় সারণির একই শ্রেণিতে মৌলসমূহের ইলেকট্রন আসক্তির পরিবর্তন ব্যাখ্যা;
গ এর উত্তর
গ্যাসীয় অবস্থায় এক মোল বিচ্ছিন্ন পরমাণুর যোজ্যতা স্তরের ইলেকট্রনের সংযোগের মাধ্যমে 1 মোল একক চার্জযুক্ত আয়ন সৃষ্টি করতে, যে শক্তি নির্গত হয় তাকে ওই মৌলের ইলেকট্রন আসক্তি বলে। মৌলের ইলেকট্রন আসক্তি একটি পর্যায়বৃত্ত ধর্ম।
পর্যায় সারণির একই শ্রেণীর যতই উপর থেকে নিচে যাওয়া যায় মৌলের পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে ইলেকট্রনের শক্তিস্তরের সংখ্যা বাড়ে পরমাণুর আকার বাড়ে। আগমনকারী ইলেকট্রন নিউক্লিয়াসের আকর্ষণ ক্রমশ কমতে, তাই মৌলের ইলেকট্রন আসক্তির মান কমতে থাকে। অর্থাৎ একটি গ্রুপের উপর থেকে নিচের দিকে মৌলের ইলেকট্রন আসক্তি কমে।
তবে হ্যালোজেন গ্রুপে ফ্লোরিন ও ক্লোরিনের ইলেকট্রন আসক্তির মানের ব্যতিক্রম রয়েছে ।যেখানে পর্যায়বৃত্ত ধর্ম অনুসারে ফ্লোরিনের ইলেকট্রন আসক্তি বেশি হওয়ার কথা ছিল ,তবে প্রকৃতপক্ষে ক্লোরিনের ইলেকট্রন আসক্তি বেশি নিচে তা আলোচনা করা হলো-
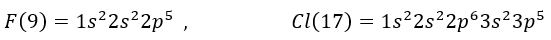
ফ্লোরিনের বহিঃস্থ দ্বিতীয় স্তরে এবং ক্লোরিনের বহিঃস্থ তৃতীয় স্তরে সাতটি করে ইলেকট্রন রয়েছে। ক্লোরিন এর তুলনায় ফ্লোরিনের আঁকা ক্ষুদ্র হওয়াতে, ফ্লোরিন এর ক্ষেত্রে বহিঃস্থ স্তরে ইলেকট্রনের ঘনত্ব অপেক্ষাকৃত বেশি বলে, আগমনকারী ইলেকট্রনের সাথে দ্বিতীয় স্তরের ইলেকট্রনের বিকর্ষণ বেশি হওয়ায় ইলেকট্রন গ্রহীতার প্রবণতা হ্রাস পায়।
ফলে ফ্লোরিনের ইলেকট্রন আসক্তি ক্লোরিনের আকারের কারণে কম। অতএব ক্লোরিনের ইলেকট্রন আসক্তি ফ্লোরিনের চেয়ে বেশি।
হ্যালোজেন গ্রুপের বাকি মৌলসমূহের ইলেকট্রন আসক্তি পর্যাবৃত্তি ধর্ম অনুসারে উপর থেকে নিচের দিকে কমতে থাকে। অতএব হ্যালোজেন গ্রুপের মৌল সমূহের ইলেকট্রন আসক্তির সঠিক ক্রম টি হবে Cl>F>Br>I
ঘ) মৌলের তড়িৎ ঋণাত্বকতার উপর বিভিন্ন নিয়ামকের প্রভাব;
ঘ এর উত্তর
কোন সমযোজী যৌগের অণুতে সমযোজী বন্ধনের শেয়ারকৃত ইলেকট্রন যুগলকে সংশ্লিষ্ট কোন পরমাণুর নিজের দিকে আকর্ষণ করার ক্ষমতাকে ওই মৌলের তড়িৎ ঋণাত্মকতা বলে। তড়িৎ ঋণাত্মকতা ও একটি পর্যায়বৃত্ত ধর্ম।
দ্বিতীয়, তৃতীয় পর্যায়ের মৌলসমূহের তড়িৎ ঋণাত্মকতার উপর নিয়ামক সমূহ যেমন পরমাণুর আকার, নিউক্লিয়ার চার্জ এবং ইলেকট্রন বিন্যাসের প্রভাব নিচে আলোচনা করা হলো:
ক. পরমাণুর আকার:
একই পর্যায়ের পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে মৌলের তড়িৎ ঋণাত্মকতার মান বাড়ে। দ্বিতীয়, তৃতীয় পর্যায়ের মৌল সমূহের যতই বাম থেকে ডান দিকে যাওয়া যায় ততই পারমাণবিক ব্যাসার্ধ কমতে থাকে ,যার ফলে শেয়ারকৃত ইলেকট্রন নিউক্লিয়াসের আকর্ষণ বৃদ্ধি পায়, ফলে তড়িৎ ঋণাত্মকতা বৃদ্ধি পায়।
দ্বিতীয় পর্যায়ের সর্বোচ্চ তড়িৎ ঋণাত্মক মৌল ফ্লোরিন এবং সর্বনিম্ন তড়িৎ ঋণাত্মক মৌল লিথিয়াম আবার তৃতীয় পর্যায়ের সর্বোচ্চ তড়িৎ ঋণাত্মক মৌল ক্লোরিন এবং সর্বনিম্ন তড়িৎ ঋণাত্মক মৌল সোডিয়াম। দ্বিতীয় তৃতীয় পর্যায়ের মৌলসমূহের তড়িৎ ঋণাত্মকতা ক্রম যথাক্রমে-
Li<Be<B<C<N<O<F Na<Mg<Al<Si<P<S<Cl
খ. নিউক্লিয়ার চার্জ:
কোন মৌলের নিউক্লিয়াসে চার্জ বৃদ্ধির সাথে সাথে তড়িৎ ঋণাত্মকতার মান বৃদ্ধি পায় ।কোন পর্যায়ের বাম থেকে ডানে যাওয়া যায়, তড়িৎ ঋণাত্মকতা ততই বৃদ্ধি পায় ।কারণ পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে নিউক্লিয়াসে ধনাত্মক চার্জ এর পরিমাণ বৃদ্ধি পায়, কিন্তু নতুন কোন ইলেকট্রন শক্তি স্তর বৃদ্ধি পায় না। এ কারণে নিউক্লিয়াসে আকর্ষণ বৃদ্ধি পায়। তড়িৎ ঋণাত্মকতার ক্রম পূর্বের ন্যায় হয়ে থাকে।
গ. ইলেকট্রন বিন্যাস:
তড়িৎ ঋণাত্মকতার উপর ইলেকট্রন বিন্যাস এর প্রভাব রয়েছে। কোন মৌলের যত বেশি ইলেকট্রন শক্তি স্তর রয়েছে ওই মৌলের তড়িৎ ঋণাত্মকতা ততকম। আর কোন মৌলের ইলেকট্রন শক্তিস্তর যত কম রয়েছে ওই মৌলের তড়িৎ ঋণাত্মকতার মান ততো বেশি হয়।
কারণ একই পর্যায়ের বাম থেকে ডানে যাওয়ার ফলে মৌলের পারমাণবিক সংখ্যা বৃদ্ধি পায়, নিউক্লিয়াসের ধনাত্মক সংখ্যা বৃদ্ধি পায়, তবে নতুন কোন ইলেকট্রন শক্তিস্তর বৃদ্ধি না হওয়ার ফলে। কেন্দ্রের নিউক্লিয়াসের প্রতি শেয়ারকৃত ইলেকট্রনের আকর্ষণ বাড়ে, যার ফলে তড়িৎ ঋণাত্মকতা ও বৃদ্ধি পায়।
বন্ধুরা এই ছিল এইচএসসি ২০২১ চতুর্থ সপ্তাহ রসায়ন ১ম পত্র অ্যাসাইনমেন্ট মৌলসমূহের শ্রেণিবিভাগ ও পর্যায়বৃত্ত ধর্ম সংক্রান্ত প্রশ্ন সমূহের সমাধান বা উত্তর। আশা করছি তোমরা মৌলসমূহের শ্রেণিবিভাগ ও পর্যায়বৃত্ত ধর্ম খুব ভালোভাবে সম্পন্ন করতে পারবে।
উত্তরদাতা, হোসাইন আহমেদ রুপন
চতুর্থ সপ্তাহে বিজ্ঞান বিভাগের অন্যান্য বিষয়ের সমাধান বা উত্তর
[ninja_tables id=”10780″]আপনার জন্য আরও কিছু তথ্যঃ
সকল স্তরের সব সপ্তাহের অ্যাসাইনমেন্ট সমূহের বাছাই করা উত্তরসমূহ দেখার জন্য নিচের বাটনে ক্লিক করে বাংলাদেশের সেরা অ্যাসাইনমেন্ট সংক্রান্ত তথ্য পাওয়ার গ্রুপে যোগ দিন। এখানে দেশের সকল প্রান্তের সেরা শিক্ষা প্রতিষ্ঠান মেধাবী শিক্ষার্থী ও অভিজ্ঞ শিক্ষকমন্ডলী নিয়মিত আলোচনার মাধ্যমে তাদের অ্যাসাইনমেন্ট সংক্রান্ত যাবতীয় সমস্যার সমাধান করছেন।